
2023年8月8日,Nature Communications杂志在线发表华中科技大学基础医学院免疫学系王维民教授团队题为“间歇性甲硫氨酸饮食缺乏促进肿瘤铁死亡并增敏免疫治疗”(Intermittent dietary methionine deprivation facilitates tumoral ferroptosis and synergizes with checkpoint blockade)的最新研究成果。研究发现,甲硫氨酸的长时缺乏和短暂饥饿对肿瘤细胞铁死亡具有截然相反的调控作用。在体内,饮食中甲硫氨酸的间歇性剥夺可显著增强肿瘤对铁死亡的敏感性,并且与PD-1抗体协同抑制肿瘤进展,增强T细胞介导的抗肿瘤免疫反应。
甲硫氨酸是一种含硫的必需氨基酸,它不仅用于蛋白质合成,而且在调控甲基化反应、含硫氨基酸代谢、维持氧化还原稳态以及信号传导等方面也发挥重要作用。由于甲硫氨酸只能从食物中获取,且很多肿瘤细胞的生长都高度依赖于外源性的甲硫氨酸,因此使得膳食甲硫氨酸限制成为一种极具潜力的肿瘤治疗策略。前期的大量研究表明,甲硫氨酸限制饮食能够抑制多种类型的肿瘤在小鼠体内的生长,并且增强肿瘤对化疗和放疗的敏感性。然而,甲硫氨酸饮食干预对靶向肿瘤铁死亡疗法以及免疫治疗的影响尚不清楚。
铁死亡是一种铁依赖的、异常脂质过氧化物累积所触发驱动的调节性细胞死亡方式。目前已发现它与肿瘤、神经退行性疾病、心血管疾病和急性肾损伤等生理病理过程密切相关。王维民教授专注于铁死亡和肿瘤免疫之间的交互调控作用,其首次发现肿瘤浸润CD8+T细胞能够抑制微环境内的胱氨酸代谢(Cell,2016),增强肿瘤细胞对铁死亡的敏感性(Nature,2019),同时提出铁死亡诱导剂协同增强PD-1抗体疗效的新策略(Cancer Cell,2021)。因此,寻找新的铁死亡诱导剂或者增敏剂,通过其靶向肿瘤细胞的铁死亡,对于肿瘤的单独治疗以及免疫联合治疗具有重要意义。
在大多数细胞中,半胱氨酸-GSH-GPX4轴是最主要的保护细胞免于铁死亡的代谢通路。细胞内的大部分半胱氨酸都来自于胞外摄取的胱氨酸,但也有少部分可通过甲硫氨酸的转硫途径生成。已有研究表明甲硫氨酸的剥夺或转硫途径的抑制可促进某些肿瘤细胞的铁死亡。王维民团队人员在前期工作中发现培养基中胱氨酸或者甲硫氨酸的单独缺乏都能降低肿瘤细胞内的GSH含量。但令人意外地是,胱氨酸单独缺乏可以显著诱导多种肿瘤细胞发生铁死亡,但甲硫氨酸的同时缺乏非但没有促进铁死亡,反而抑制了胱氨酸缺乏诱导的铁死亡。同样的,甲硫氨酸缺乏也能显著抑制erastin诱导的铁死亡。之后检测细胞内的GSH含量发现,甲硫氨酸的缺乏逆转了胱氨酸缺乏导致的GSH下降。更有意思的是,当作者对肿瘤细胞进行短暂的(£8h)甲硫氨酸饥饿预处理后再给予胱氨酸单独缺乏的处理,反而促进了肿瘤细胞的铁死亡,同时促进了细胞内GSH含量的下降。综上,甲硫氨酸的长时缺乏和短暂饥饿对肿瘤细胞铁死亡具有截然相反的调控作用。
同时作者对上述现象背后的分子机制进行了深入研究。在胱氨酸剥夺或erastin诱导的铁死亡过程中,会伴随CHAC1蛋白的从头合成,后者能够增强GSH的降解并促进铁死亡的发生;但甲硫氨酸的长时缺乏会抑制CHAC1的蛋白合成,从而抑制铁死亡的发生。与长时缺乏不同,甲硫氨酸的短暂饥饿则只会促进CHAC1的转录而不抑制其蛋白翻译,因此会增强GSH的降解和铁死亡的发生。
基于此,作者提出间歇性的甲硫氨酸饮食缺乏会有利于体内肿瘤细胞铁死亡的发生。实验结果显示,间歇性甲硫氨酸饮食缺乏能够显著增强铁死亡诱导剂IKE的抗肿瘤活性,并且该饮食方案单独处理就会抑制肿瘤生长。进一步,作者还探索了间歇性甲硫氨酸饮食缺乏与PD-1抗体在体内的联合治疗效果。结果显示二者联合能够显著抑制肿瘤的生长并增强T细胞免疫应答,且联合治疗效果显著优于单独治疗。而且上述治疗效果依赖于肿瘤细胞中CHAC1的表达。在进行了免疫治疗的黑色素瘤患者标本中,作者发现CHAC1的高表达与治疗的响应性和病人生存率呈正相关。最后,作者发现使用间歇性甲硫氨酸饮食缺乏、铁死亡诱导剂IKE和PD-1抗体的三重组合疗法,可以进一步抑制肿瘤进展并延长荷瘤小鼠的生存期。
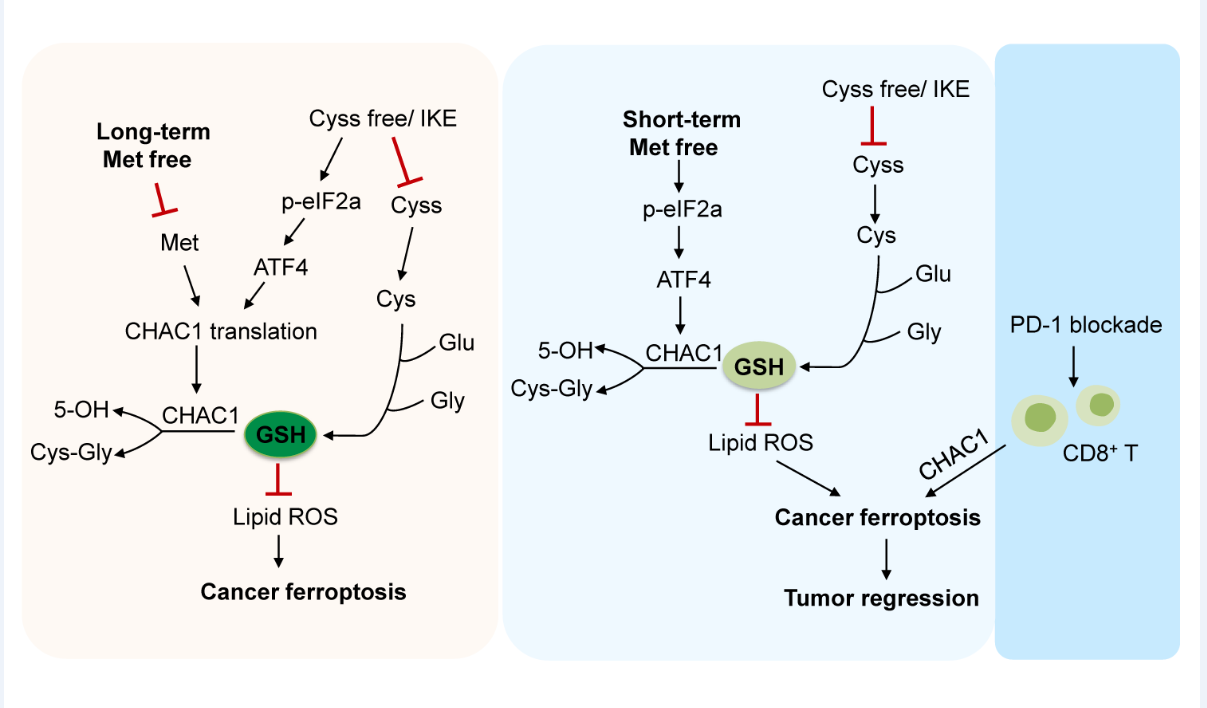
甲硫氨酸的长时缺乏和短暂饥饿对铁死亡的不同调控作用
综上所述,这项研究深入揭示了甲硫氨酸对细胞铁死亡调控作用的两面性,阐明了甲硫氨酸代谢、肿瘤铁死亡和抗肿瘤免疫反应之间的相互作用,革新了人们对于特殊饮食在体内生理条件下调控组织细胞死亡和免疫反应的理解和认知,为饮食干预氨基酸代谢用于肿瘤治疗的临床转化奠定了理论基础。
华中科技大学基础医学院免疫学系王维民教授为该论文的通讯作者,免疫学系博士研究生薛莹和吕付佳老师为该论文的共同第一作者。该研究工作得到了国家自然科学基金青年及面上项目、科技部重点研发计划项目、湖北省自然科学基金杰出青年项目和华中科技大学自主创新基金的支持。
原文链接:
https://www.nature.com/articles/s41467-023-40518-0
 学院官方微信
学院官方微信