2024年2月1日,华中科技大学基础医学院生物化学与分子生物学系研究生李能同学和团队成员在国际著名期刊The Journal of Biological Chemistry(Nature指数期刊、美国生物化学与分子生物学学会会刊)发表了题为“在肝癌中P53-P21-RB1轴通过USP1促进BRD4蛋白的降解”(The P53-P21-RB1 pathway promotes BRD4 degradation in liver cancer through USP1) 的研究论文,阐述了在肝癌中P53如何促进BRD4蛋白的降解,有助于开发 BRD4 靶向疗法。

肝癌是全球发病率第五高的癌症,也是导致癌症相关死亡的第四大原因。癌症的发展依赖于癌症驱动基因的激活和/或过度表达。BRD4 被认为是这些癌症驱动基因的主要激活剂之一。BRD4是 Bromodomain and extra-terminal (BET) 家族成员蛋白,BRD4 通过其 N 端的Bromodomain识别乙酰化的组蛋白。同时,BRD4 与基因特异性转录因子和包括mediators在内的一般转录激活蛋白相互作用。BRD4 与DNA上的启动子或增强子元件结合,通过与其他蛋白的相互作用促进癌症驱动基因的转录。BRD4的靶基因因细胞类型而异,并执行不同的功能,包括细胞增殖、代谢和免疫逃逸。因此,BRD4 已成为一个很有前景的治疗靶点,超过70项临床试验已经开展或正在开展。针对 BRD4 的创新疗法,包括更强/更特异的抑制剂和降解诱导剂也是研究的热点。BRD4的蛋白表达在多种癌症中高表达,但是其机制仍不完全清楚。
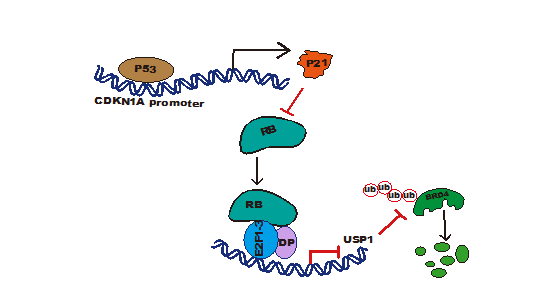
李能同学所在团队长期研究表达遗传修饰相关蛋白质在癌症中的表达调控和生物学功能。在本研究中,李能同学等人首先通过数据库分析,发现在肝癌样本中野生型P53 和 BRD4 蛋白水平之间有很强的负相关。通过BRD4敲低实验,发现BRD4敲低可以削弱由于P53敲低而导致的肝癌细胞的增殖。又通过在肝癌细胞中过表达野生型P53,在P53野生型肝癌细胞系中敲低P53,P53激活剂处理等实验证明P53蛋白可以降低BRD4蛋白的稳定性。接着作者证明P53对BRD4的调控是通过泛素蛋白酶体途径。李能同学等检测了P53是否是通过BRD4已报道的去泛素化酶或泛素连接酶来影响BRD4的蛋白水平。结果表明P53不是通过这些蛋白来调节BRD4的蛋白水平。随后李能同学等筛选鉴定发现了BRD4新的去泛素化酶USP1,之后证明USP1与BRD4存在相互作用。又通过对USP1基因的敲低和过表达,及体内与体外的去泛素化实验证明了USP1在肝癌细胞中可以去除BRD4蛋白上的泛素分子,从而增强了BRD4蛋白的稳定性。李能同学等又通过CCK8,克隆形成,异种移植瘤等实验,证明了USP1对肝癌细胞增殖的影响部分是通过BRD4来发挥作用。鉴于BRD4 作为转录调控因子的重要作用,为了深入了解其潜在机制,李能同学等接下来用 RNA-seq分析了 USP1-BRD4 轴如何调控肝癌细胞转录组。敲低 USP1 或 BRD4 会导致 100 多个基因的表达发生显著变化,且USP1-KD 下调的基因和 BRD4-KD 下调的基因之间存在明显的重叠。同样,基因富集分析表明,USP1 和 BRD4 也调控共同的通路。后续的机制探究表明P53可以通过P21-RB1轴抑制USP1基因的表达,从而影响BRD4蛋白的稳定性。该研究揭示了P53这一重要的抑癌基因和BRD4之间的联系。该研究所揭示的机制有助于开发靶向 BRD4 的疗法,也为携带P53突变的肝癌患者提供新的治疗思路。
生物化学与分子生物学系博士研究生李能及华中科技大学附属同济医院张二雷博士为该论文的共同第一作者,生物化学与分子生物学系宋檀婧和孙立栋老师为共同通讯作者。该研究得到了国家自然科学基金的支持。
 学院官方微信
学院官方微信