
2025年7月22日,华中科技大学同济医学院基础医学院郭峥教授团队在 Nature communications 上发表题为“Age mosaic of gut epithelial cells prevents aging”的研究论文。该研究揭示了果蝇肠道上皮细胞通过形成年龄镶嵌改善肠道健康、延长寿命。
果蝇因生命周期短、繁殖快,是研究衰老的理想模式生物。随着衰老,其肠道中出现肠道干细胞(ISC,intestinal stem cell)过度增殖和肠道屏障泄漏,最终引起个体死亡。然而,衰老过程中ISC过度增殖的触发机制仍不明确。此外,早期损伤(Early Injury, EI)会刺激ISC分裂产生新的肠道上皮细胞(enterocyte,EC)替代受损的EC。然而早期损伤对衰老果蝇肠道的生理状态、寿命及ISC过度增殖的影响尚未得到深入研究。
在本项研究中,作者发现早期损伤(EI)延长了果蝇寿命(图1a)。在逐日统计ISC的增殖趋势时,作者发现对照组UT肠道中ISC的过度增殖并非线性发生,而是在约20天(25℃)时突然发生;而EI缓解了这一衰老过程中ISC过度增殖的发生(图1b)。
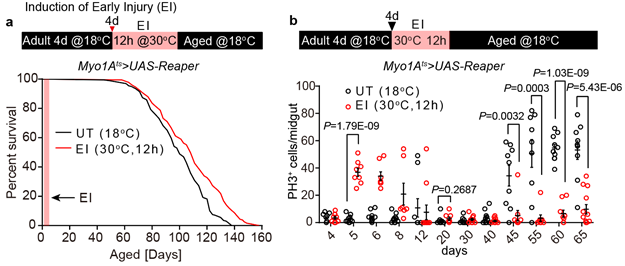
图1早期损伤延长果蝇寿命并阻止了衰老时ISC的过度增殖
a-b,早期损伤延长了果蝇寿命。b,早期损伤缓解了衰老时ISC的过度增殖的突然发生。
那么为什么对照组肠道会在20天左右突然发生ISC的过度增殖,而早期损伤则避免了这些突然变化?为了解析早期损伤缓解衰老时ISC过度增殖的分子机制,该团队逐日将UT组和EI组果蝇肠道RNA进行转录组测序。逐日的肠道转录组测序明确了肠道衰老的非线性进程:UT组热图显示,从第4天到第18天肠道转录组基因表达无显著变化,但在18天到19天之间发生了突然剧烈的变化,并从19天开始呈现出衰老肠道的基因表达模式(图2b)。然而,EI组的基因表达水平在19天没有出现显著变化(图2b),说明早期肠道损伤避免了在UT组在19天突然出现的转录组变化。
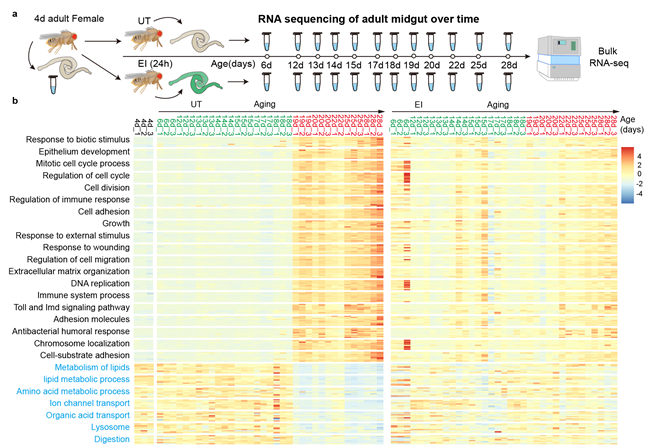
图2早期损伤避免了果蝇第19天时出现转录组的突然变化
a,果蝇肠道转录组测序流程图。b,按时间顺序将UT组和EI组果蝇肠道转录组中差异表达最显著的基因从4天到28天进行表达水平的热图分析。
那么,是什么导致UT组在衰老时出现肠道转录组的剧烈变化呢?该团队通过短暂表达H2B-RFP蛋白来标记和追踪肠道EC,发现蛹期肠道发育过程中同时产生的EC随着衰老不断累积ROS和降解核膜蛋白Lamin,在常温下20天左右触发EC的集体性更替,引起了ISC的过度增殖。而早期损伤激活ISC增殖生成了新的EC;这些新产生的EC嵌入蛹期肠道产生的‘老’的EC群体,从而在肠道上皮中形成新和老EC年龄镶嵌(age mosaic)的分布模式,新-老EC的有序更替避免了衰老时EC集体性更替,从而缓解了衰老时ISC过度增殖。
为什么一旦发生EC集体更替时会持续产生ISC的过度增殖,而早期损伤形成EC的年龄镶嵌却能避免ISC过度增殖的发生?该团队发现,当EC集体更替时不能形成完整的细胞间隔膜连接(septate junction, SJ),导致肠道屏障功能受损,引发持续的ISC过度增殖(图3);而EC的年龄镶嵌避免了衰老时EC集体更替,重塑了EC间的SJ,进而阻止了ISC的过度增殖(图3)。
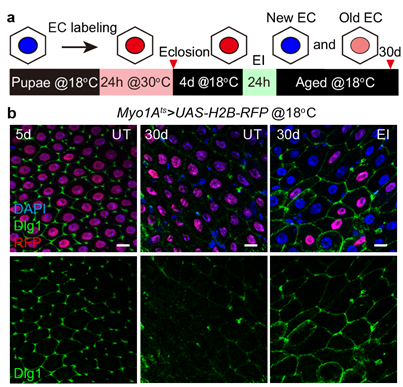
图3年龄镶嵌改善了衰老时EC间的隔膜连接
a,在果蝇蛹期肠道短暂诱导H2B-RFP的表达来标记和追踪EC并检测EC间的隔膜连接的示意图。b,相对于5天时UT组RFP+EC间的隔膜连接蛋白组分Dlg1的较高表达水平,30天时UT组RFP+EC之间的Dlg1的表达强度显著减弱。但是与UT组30天时肠道EC之间的Dlg1表达相比,30天时EI组EC之间Dlg1的表达水平均显著增强。
与自由进食(ad libitum, Ad)相比,限时性间歇性禁食(intermittent time-restricted feeding , iTRF)能够缓解果蝇衰老时肠道的ISC过度增殖,并显著延长果蝇的寿命。该团队发现iTRF通过激活EC自噬诱导EC形成年龄镶嵌,从而改善肠道EC之间的隔膜连接、缓解衰老肠道中ISC的过度增殖并延长寿命(图4)。
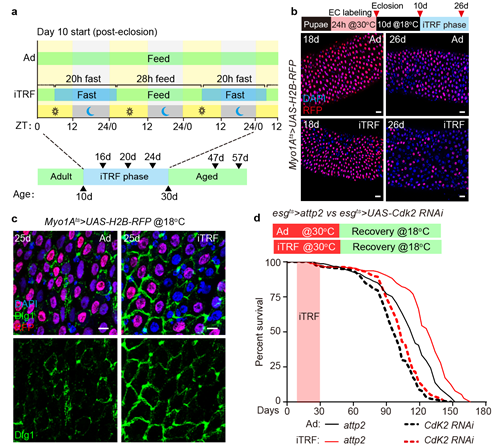
图4 iTRF通过诱导EC的年龄镶嵌改善肠道健康并延长寿命
a,对果蝇进行自由进食(ad libitum,Ad)和限时性间歇性进食(intermittent time-restricted feeding,iTRF)处理的示意图。b-c,iTRF诱导EC的年龄镶嵌改善了EC间的SJ。d,阻止EC形成年龄镶嵌削弱了iTRF调控的寿命延长。
综上所述,该项研究发现了早期损伤或间歇性禁食诱导肠道上皮形成年龄镶嵌,缓解了衰老时ISC的过度增殖,改善了肠道上皮细胞间的隔膜连接并延长果蝇寿命。该研究从组织中细胞年龄构成的角度解析了器官或个体的衰老,并发现年龄镶嵌可以逆转衰老的进程。这项研究提示在器官和组织中形成细胞间的年龄镶嵌即可成为逆转衰老的一种策略,而不仅限于清除衰老细胞(senescence cells)。
华中科技大学基础医学院医学遗传系郭峥教授为该论文的通讯作者,医学遗传系博士生秦培忠为该论文第一作者。该工作得到国家自然科学基金委的项目支持。
文章链接:https://rdcu.be/exkT1
 学院官方微信
学院官方微信