肿瘤细胞对于CD8+T细胞的免疫逃逸使得现有的免疫疗法对许多癌症患者的疗效不佳。如何使肿瘤细胞变得“脆弱”、更容易被T细胞识别和杀伤?团队的前期研究发现铁死亡(ferroptosis)是CD8+T杀伤肿瘤的新机制。通过靶向肿瘤细胞铁死亡能够显著增强免疫检查点抑制剂的治疗效果。铁死亡是一种由膜脂质过氧化驱动的细胞死亡方式,其发生与细胞内膜系统密切相关,包括内质网、线粒体、溶酶体在内的膜性细胞器已被证实参与脂质过氧化的起始、放大与传播过程。然而,高尔基体作为负责蛋白质与脂质加工分选的关键膜结构细胞器,其与铁死亡的关系并不清楚。高尔基体如何响应铁死亡压力?如何调控铁死亡结局?这些问题此前尚未被揭示。
2026年4月21日,华中科技大学同济基础医学院王维民教授团队在Nature Cancer杂志上发表了题为TMEM87A suppresses ferroptosis and increases cancer immunotherapy resistance by maintaining the Golgi apparatus pH homeostasis的研究论文,揭开了高尔基体参与铁死亡调控的神秘面纱。

研究团队首先发现:在铁死亡早期高尔基体膜上出现快速脂质过氧化物累积,并导致高尔基体pH升高。通过筛选锁定了高尔基体跨膜蛋白TMEM87A ,作为离子通道通过维持高尔基体pH稳态抵抗铁死亡。进一步的机制研究表明,TMEM87A缺失通过抑制经典的铁死亡防御蛋白FSP1的功能,使还原型辅酶Q(CoQH₂)水平下降,降低细胞还原过氧化脂质的能力,从而增敏肿瘤细胞铁死亡。此外,团队还在多种小鼠肿瘤模型上证实:TMEM87A缺失通过促进肿瘤铁死亡抑制肿瘤进展,增强CD8⁺ T细胞免疫应答,并提高PD-1抗体疗效。进一步分析临床样本,发现TMEM87A高表达与黑色素瘤、肺癌患者的免疫治疗响应不佳及总生存期缩短显著相关。
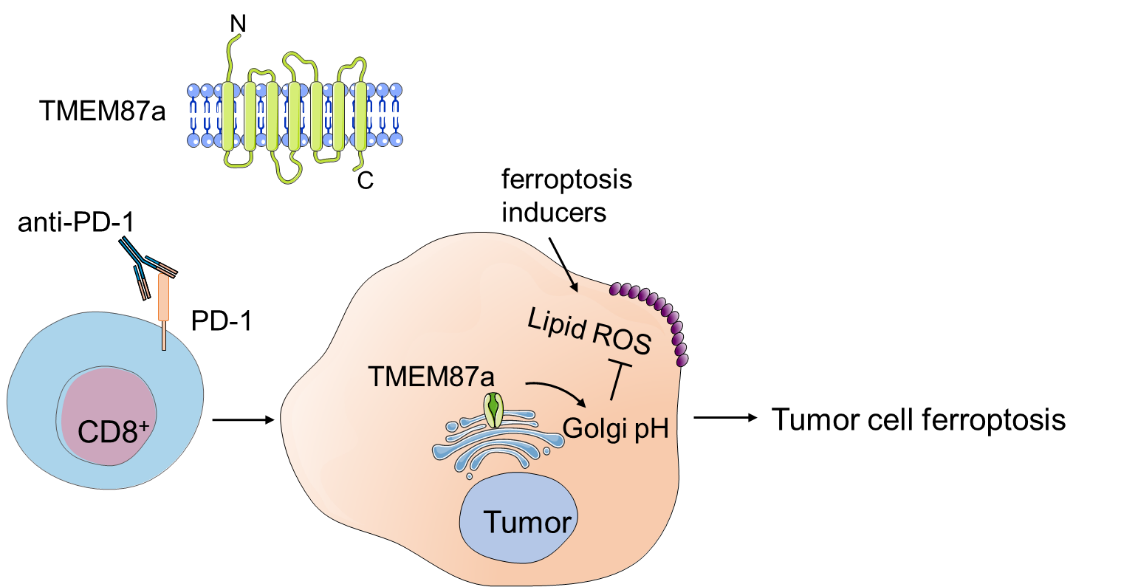
综上所述,该研究首次系统地阐明了高尔基体及其驻留蛋白TMEM87A在调控细胞铁死亡和抗肿瘤免疫中的关键作用。该发现不仅拓展了对铁死亡亚细胞调控网络的认知,也为开发基于靶向TMEM87A的肿瘤联合治疗策略提供了理论依据。由于明确了高尔基体上调控铁死亡的离子通道TMEM87A,未来可以筛选靶向该通道活性的小分子抑制剂,从而用于铁死亡的调控和免疫治疗的增效。此外,对临床样本的分析表明TMEM87A高表达提示生存期更短,且对免疫治疗响应更差,因此TMEM87A的表达也可能作为预测免疫治疗响应性的生物标志物。
华中科技大学基础医学院王维民教授为本文独立通讯作者。华中科技大学基础医学院博士后李经和博士研究生周瑀涵为共同第一作者。该研究工作得到了国家自然科学基金、科技部重点研发计划项目、湖北省自然科学基金和华中科技大学自主创新基金的支持。

 学院官方微信
学院官方微信
