以侵袭性念珠菌病为代表的深部真菌感染,已成为全球公共卫生领域面临的重大挑战。其中,耳念珠菌(Candida auris)因其快速传播、多重耐药和高致死率,已成为当前最受关注的致病真菌之一。该病原对唑类药物具有天然耐受性,并常对多类临床一线抗真菌药物产生耐药,感染后的病死率可高达30%–60%,因此被称为“超级真菌”。鉴于其严重危害,世界卫生组织(WHO)已将耳念珠菌列入“严重优先级”真菌病原体,凸显了开发新型靶点与靶向药物的迫切需求。糖基磷脂酰肌醇锚定蛋白(glycosylphosphatidylinositol-anchored proteins, GPI-APs)是真菌细胞壁蛋白中最主要的一类,广泛参与细胞壁构建、黏附侵袭、毒力维持等关键过程。其生物合成通路已成为抗真菌药物研发的重要方向,目前已有多个靶向药物进入研发阶段,显示出良好的应用前景。因此,深入解析耳念珠菌GPI锚定蛋白生物合成的分子机制,对于发展新型抗真菌策略具有重要意义。
2026年3月23日,华中科技大学同济医学院基础医学院于洪军、张敏团队联合南方科技大学生命科学学院张明杰院士、刘晓天研究员团队在Protein & Cell杂志上发表题为Molecular insights into Candida auris glycosylphosphatidylinositol transamidase的文章。该研究围绕GPI锚定蛋白合成过程中关键的转酰胺反应,系统解析了耳念珠菌GPI转酰胺酶(GPI-T)五亚基复合体的组装模式、底物识别和催化特征,并揭示了其与人源同源复合体之间的重要种属差异,为开发高选择性的抗真菌药物提供了重要分子依据。

研究基于人源PIGK/PIGT/PIGS/PIGU/GPAA1基因敲除细胞系,以CD59作为功能报告分子,建立了基于流式细胞术的耳念珠菌GPI-T功能重建与检测体系,克服了致病真菌GPI合成研究中缺乏实验体系以及耳念珠菌基因编辑困难等难题。利用该体系,研究发现耳念珠菌GPI-T任一单独亚基均无法与人源对应亚基互相替代,只有完整的五亚基才能有效恢复功能活性。这表明该复合体的功能组装对亚基完整性具有严格依赖性,同时也凸显了其与人源系统之间显著的种属特异性。研究进一步捕捉了耳念珠菌GPI-T结合内源性GPI底物的状态,揭示了其以稳定的五亚基复合体形式存在,其整体装配依赖于广泛的亚基间相互作用以及Gab1与Gaa1之间的脂质介导接触。研究明确鉴定出由Gab1、Gpi16和Gaa1共同构成的保守GPI结合位点,阐明了GPI-T复合体对底物的精确识别机制。与人源同源复合体的系统比较进一步发现,两者在多个关键亚基互作界面处存在显著差异,解释了功能重构研究中发现的种属间功能不兼容性。特别的,研究揭示催化亚基Gpi8中存在显著的真菌特异性分子特征,包括一个参与蛋白底物结合的特异性loop区,以及一个对催化活性至关重要且在真菌中保守的C端锚定Loop1区域。这些关键元件在人源同源蛋白中并不保守,提示其可能构成病原真菌特异性药物设计的潜在切入点。
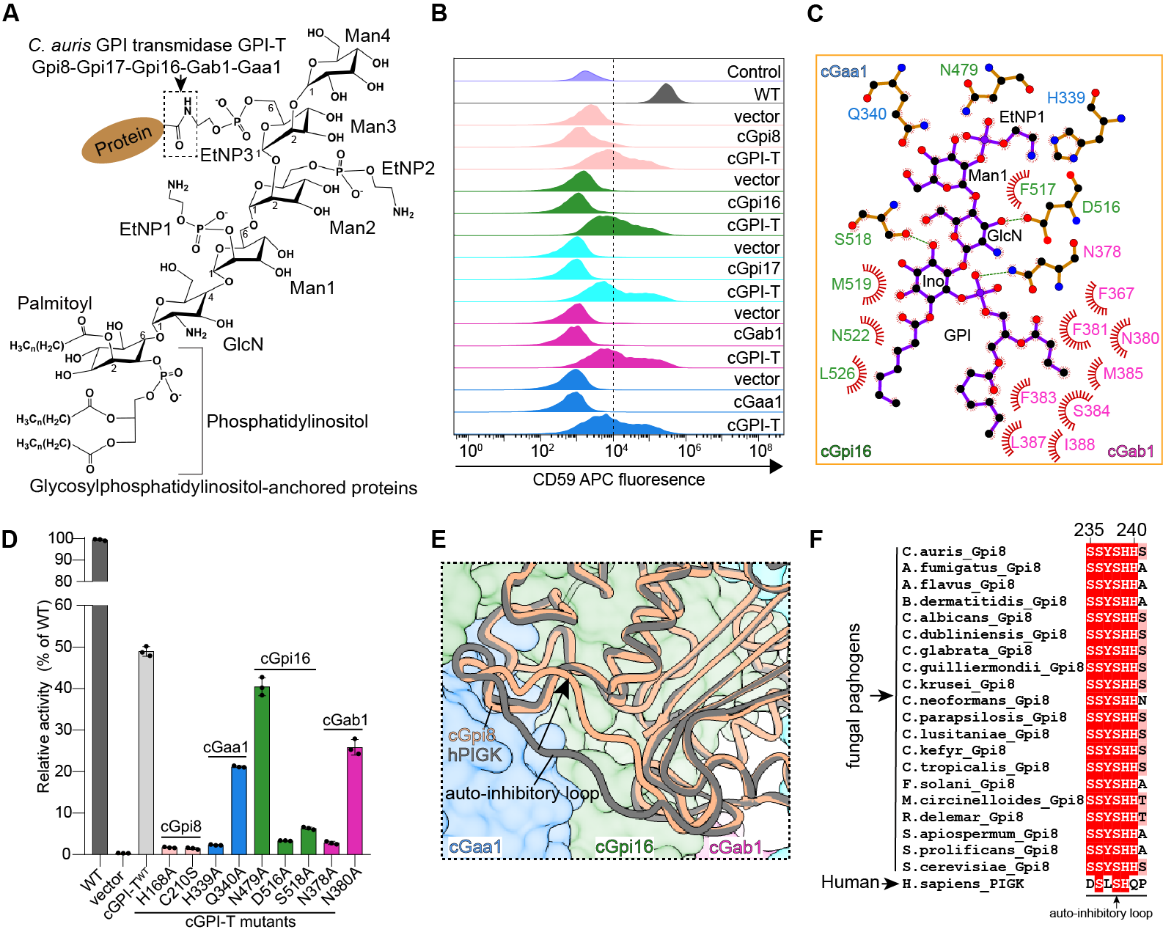
图1:耳念珠菌GPI transamidase GPI-T的功能机制研究
综上所诉,本研究系统阐明了耳念珠菌GPI-T复合体的分子机制,解析了其组装模式、底物识别策略以及与宿主-病原之间的关键差异,不仅深化了对致病真菌GPI锚定蛋白生物合成的认识,也为基于种属差异的抗真菌药物理性设计提供了重要依据。
华中科技大学基础医学院于洪军教授和张敏副研究员、南方科技大学的刘晓天副研究员为本文共同通讯作者。华中科技大学基础医学院博士研究生丁旭扬和华正康为共同第一作者,华中科技大学基础医学院为第一完成单位。江南大学柳艺石教授为研究提供了重要支持。本研究得到了国家自然科学基金等项目的资助和支持。
原文链接:https://doi.org/10.1093/procel/pwag023
 学院官方微信
学院官方微信