
2023年10月23日,华中科技大学基础医学院宇兴江课题组在Neuro-Onoclogy上发表了题为“FAM129A通过稳定胶质瘤干细胞中的Notch细胞内结构域促进自我更新并维持侵袭状态”(FAM129A promotes self-renewal and maintainsinvasive status via stabilizing the Notch intracellulardomain in glioma stem cells)的研究论文,阐释了胶质瘤干细胞侵袭新机制。
恶性神经胶质瘤(Glioma),尤其是胶质母细胞瘤(GBM),是中枢神经系统的主要致死性肿瘤。GBM的异质性和可塑性是导致其耐放化疗和术后复发的关键因素。这些恶性特征被认为起源于胶质瘤干细胞(GSCs,一种具有自我更新和致瘤能力的肿瘤细胞亚群)。GBM与其它实体瘤的主要区别在于具有广泛浸润周围脑组织的能力,但很少转移到其它器官。残留或远处迁移的GSCs的浸润潜力阻碍了手术切除的疗效并导致复发。
FAM129A,是一种内质网应激相关蛋白,可调节eIF2a和S6K1/4E-BP1的磷酸化以调控细胞死亡。FAM129A在几种癌症中上调,包括肾癌、前列腺癌,甲状腺癌和肝细胞癌等。
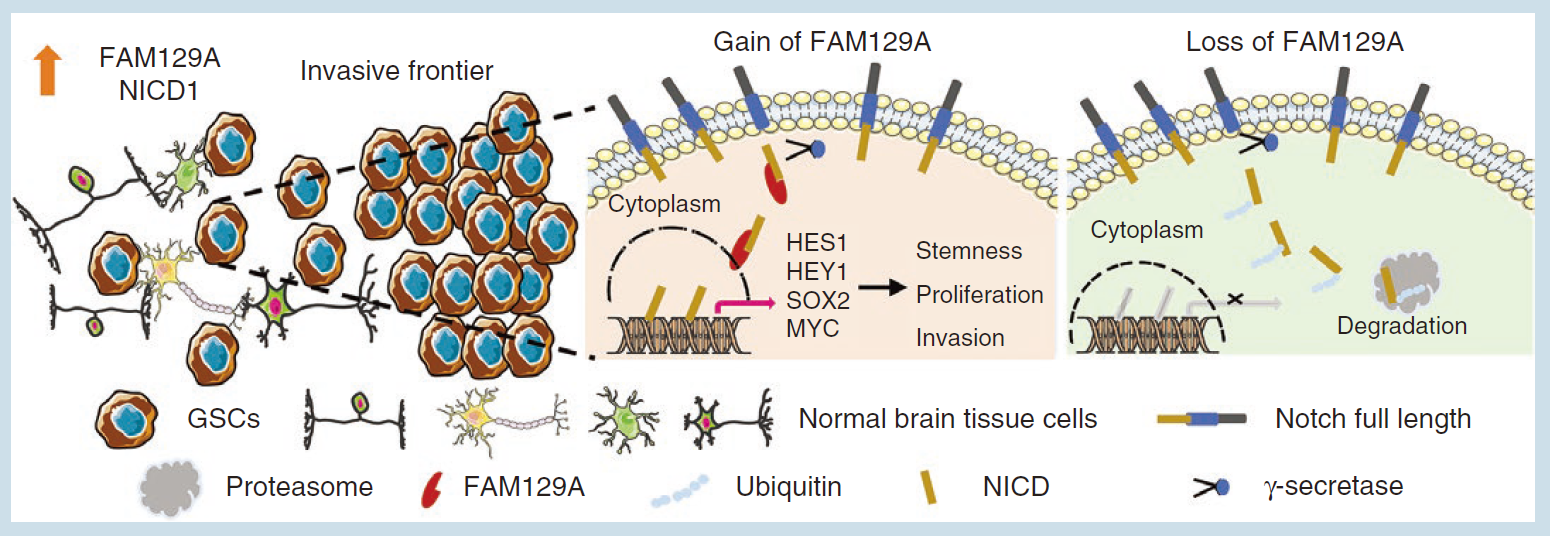
研究人员首先阐明了GBM组织中浸润性GSCs至少有三种侵袭模式:血管周围浸润、集体浸润和沿髓鞘浸润,并且具有独特的时空基因表达特征。经生物信息学及实验确定FAM129A为候选基因。进一步发现FAM129A优先表达于GSCs中,与侵袭性GSC高度相关;通过不依赖凋亡的途径调控SOX2的表达方式维持GSC自我更新,并且能促进GSCs的侵袭和迁移。最后研究人员阐明了FAM129A对GSCs及GBM的恶性调控机制是通过与NICD1结合防止其被泛素化降解并激活Notch信号通路来实现的。
综上所述,这项研究表明,FAM129A在GBM侵袭区域表达增加,FAM129A的下调损害了GSCs的自我更新和致瘤潜力,阻止了其浸润到正常脑实质中。因此,FAM129A对于维持GSC的浸润潜力至关重要,并可作为GBM的治疗靶点。
华中科技大学基础医学院组胚系宇兴江研究员和同济医院神经外科郭东生教授为该论文的共同通讯作者,同济医院神经外科硕士生刘国豪和博士生张泼为该论文第一作者。该研究工作得到了国家自然科学基金、华中科技大学学术前沿青年队项目以及华中科技大学自主创新基金的支持。
